
An diesem Kurstag sollte die Frage geklärt werden, welcher Mechanismus galaktische Emissionsnebel zum Leuchten bringt. Im Gegensatz zu Sternen, deren Farbe über die Planck’sche Theorie der Schwarzkörperstrahlung erklärt werden kann, gibt es für das Leuchten galaktischer Nebel einen ganz anderen Grund…
Das Leuchtspektrum von Sternen weist (neben charakteristischen Peaks) einen kontinuierlichen Verlauf auf. Es bestitzt an einer bestimmten Frequenz (Lichtfarbe) ein Maximum, dessen Intensität und Position von der Temperatur der Sternoberfläche abhängt – die Schwarzkörperstrahlung.
Bei leuchtenden galaktischen Emissionsebeln, die vornehmlich in einem geheimnisvollen Rot vor sich hin dämmern, liegt ein ganz anderer Grund vor. Die Ursache kann nur mit den Erkenntnissen aus der Quantentheorie erklärt werden (wie seltsamerweise ebenfalls die o.g. Schwarzkörperstrahlung!). Galaktische Gaswolken bestehen vornehmlich aus Wasserstoff. Es ist elektrisch neutral; sein Atomkern ist ein einzelnes Proton, welches von einem Elektron ‚umkreist‘ wird. Nach den Gesetzen der klassischen Elektrodynamik müsste das Elektron bei seiner Bewegung um den Atomkern eigentlich elektromagnetische Wellen abstrahlen. Dies würde zu einem Energieverlust des Elektrons führen – mit der Konsequenz, dass es schließlich auf den Atomkern prallte.
Dass das Elektron jedoch auf seiner Bahn verbleibt und keine elektromagnetischen Wellen erzeugt, hat quantenmechanische Gründe. Denn es hält sich Wirklichkeit in einem diskreten Energieband auf, einem von unendlich vielen Energiebändern, und ist so vom Proton im Atomkern gefangen. Das Elektron kann jedoch von einem Energieband in ein anderes wechseln. Will es in ein höheres Energieband aufsteigen, so benötigt es Energie; z.B. in Form von Strahlung. Dort kann es dann eine Weile verbleiben.
Wenn kein weiterer Energieschubs erfolgt, der es noch weiter noch oben auf der Energieleiter oder – bei der Ionisation sogar außerhalb – befördern würde, kann das Elektron auch wieder in eine niedrigere Energiestufe zurückspringen. Hierbei wird Energie in Form von Strahlung freigesetzt. Je höher der Unterschied der Energiestufen ist, desto höher wird die abgestrahlte Energie und damit (nach der Planck’schen Formel E=h*f) die Frequenz (Farbe) des Photons!
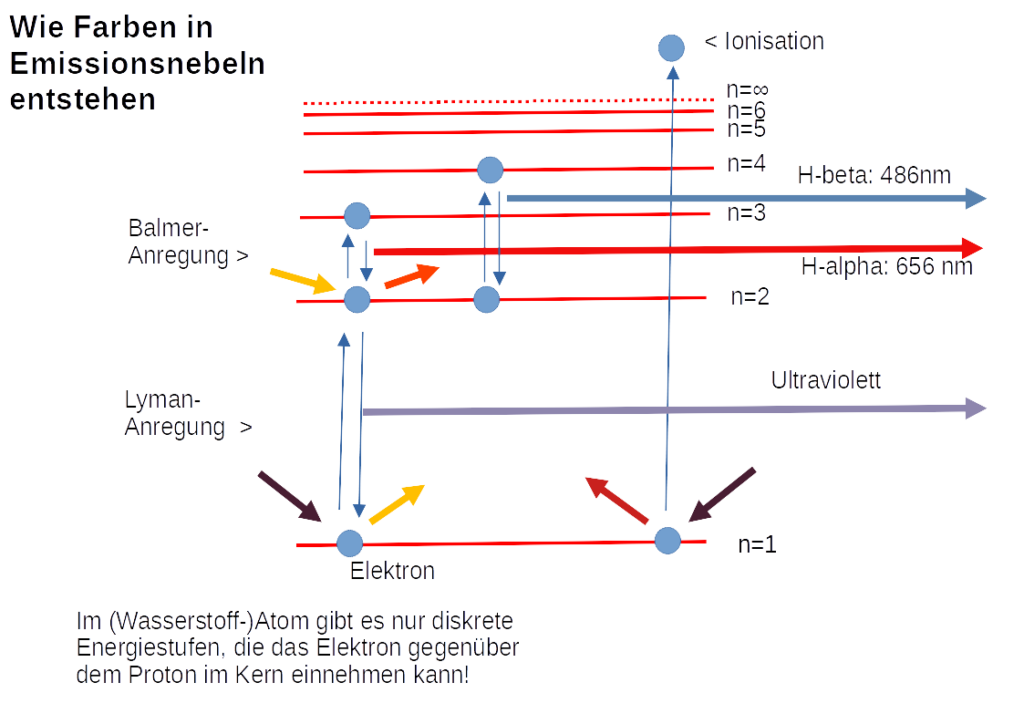
Das Licht, das beim Zurückfallen von höheren in niedrigere Energiestufen von menschlichen Auge wahrgenommen werden kann, ist der Rückfall auf die zweite Stufe (Balmer Serie, n=2). Die geringste Energiemenge, die abgestrahlt werden kann, erfolgt dabei von der dritten in die o.g. zweite Stufe. Dies entspricht einem Lichtquant mit der Wellenlänge von 656 nm – dem H-alpha-Licht!
Das andere sichtbare Licht, welches von einem Wasserstoffatom abgestrahlt werden, kann ist der Rückfall von der vierten in die zweite Stufe. Es ist blau leuchtendes H-beta-Licht. Blau-Violettes und Violettes Licht wird von der 5. bzw. 6. Energiestufe in die 2. Energiestufe freigesetzt (H-gamma und H-delta- Licht).
Bei alle ‚Rückfallstufen‘ auf das niedrigste 1. Level (n=1) erzeugt Photonen im Ultravioletten; also für das Auge nicht sichtbares Licht.
Entsprechende Prozesse finden auch in Gaswolken mit anderen chemischen Zusammensetzungen statt, die z.B. Bestandteile von Sauerstoff oder Stickstoff enthalten. Diese leuchten dann ebenfalls in ihren spezifischen Farben, im Ultravioletten oder auch im Infraroten.
Wie man sieht, entsteht Licht in galaktischen Emissionsnebeln auf einem gänzlich anderen Wege wie das Licht bei der Temperaturstrahlung von Sternen. Doch es gibt etwas, das beides miteinander verbindet: Es kann nur unter der Annahme funktionieren, dass Licht in Energiepaketen, sogenannten Lichtquanten (Photonen) abgestrahlt wird. Planck sein Dank!


